透射电镜生物样品的制备技术比较多,比如超薄切片技术、负染色技术、免疫电镜技术、电镜细胞化学技术等,其中超薄切片技术是最具基本、最常用的制备技术其它一些样品制备技术都离不开超薄切片的制作。利用透射电镜观察超薄切片,可以了解细胞的精细结构,下面主要介绍一下超薄切片的制备。
首先了解一下超薄切片的要求:
超薄切片需要达到以下的基本要求:
1、细胞的精细结构保存良好
2、切片厚度必须小于100nm,常用的是50~70nm
3、切片能耐受电子束的强烈照射
4、切片有良好的反差
5、切片均匀,无褶皱、刀痕和污染
超薄切片的制作过程:
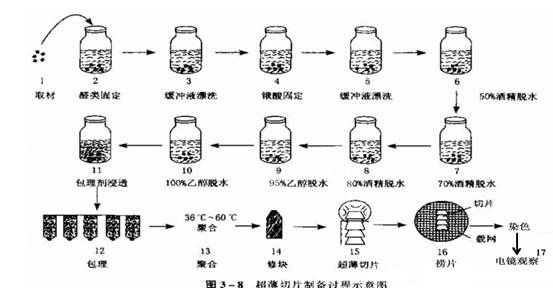
1、 取材2、醛类固定3、缓冲液清洗4、锇酸固定5、缓冲液清洗6—10酒精丙酮脱水11、包埋剂浸透12、包埋13、聚合14、修块15、超薄切片16染色。
整个过程下来至少要7到10天的时间(由于单个用户一次的样品量一般比较少,所以我们电镜室一般是收到10粒以上样品才集中处理包埋,这之间会有一定的时间差,用户要提前预留出一定时间如果特别着急,需提前咨询看时间能否调整)
详细流程及时间安排:
1、 醛类固定几小时或者更长时间
2、 缓冲液清洗3次,中间一次过夜
3、 俄酸后固定90分钟左右根据样品不同略微调整
4、 缓冲液清洗3遍每次15分钟
5、 乙醇剃度脱水分别用50%、70%、90%各一次每次15分钟,100%3次,每次15分钟。丙酮2次一共15分钟。
6、 包埋剂浸透,梯度浸透,分别用丙酮和包埋剂3:1、1:1、1:3浸透几个小时最后纯包埋剂浸透过夜。
7、 集合先经37℃与45℃各加温12小时,然后再在60℃下加温48小时
8、 聚合成包埋块,进行修快、半薄切片定位、再切超薄切片。
9、 用醋酸双氧铀和柠檬酸铅染色
10、 上电镜观察。
对各步骤分别做详细介绍:
一、 取材
取材是由研究生或科研人员亲自操作的。
在取材的过程中出现的问题比较多,如果方法不正确将导致实验结果的失败,所以电镜取材是整个样品制备过程中的关键步骤之一。
取材前的准备工作:
1、明确实验目的、制作实验流程
2、选择好实验动物或细胞、试剂、器具、器皿(除了解 剖用的,电镜需要、青霉素小瓶、双面刀片、硬纸板、牙签、冰块)
3、取材的器官、部位一定要事先了解(一定要有解剖学知识,对所有器官非常了解,取之前要考虑周密)
4、必须设立对照组,取材的条件、部位完全相同,时间上尽量保持同步。
取材的基本要求:
快 动作要熟练、取材要快速,力争样品离体后在1分钟内进入预冷固定液中
准 取材部位要准确,肾脏、胰岛、垂体等不同部位有不同结构和功能,应根据研究目的和要求确定切取部位。为了便于比较,各组动物取材部位应一致。
冷 为了降低细胞内酶的活性,减少组织自溶,取材最好在低温条件下进行
小 组织块体积应小于1mm3。对于较难一次性取小的组织,可先适当取大一点,投入4%多聚甲醛中固定,随后取出切成小块,再放入戊二醛固定液中继续低温固定。
少 所用器械应锋利,取材时应避免牵拉、挤压,减少人为造成的组织损伤
净 取材所需器械、容器必须干净
动物取材方法:
动物麻醉或立即处死,暴露所需的脏器,在不中断血液供应的情况下用锋利剪刀剪下一小块组织,迅速放到滴有预冷固定液的硬纸片上,在固定液中用刀片切去剪过的切面,把组织切成薄片,再改切成体积约1mm3小块或横切面约 1 mm2 、长约2mm的长条形(需定位的组织,如大脑皮层、肾皮质等),用牙签将4-5块组织转移至含有2-3ml预冷固定液的青霉素小瓶内,瓶上应贴上标签(用铅笔书写),置于4℃冰箱内固定、保存。
取材过程耗时长、操作复杂或特殊组织(如脑组织、眼球等),可以采用动物灌注固定后再行取材。对于动物组织取材,都建议采取灌注固定后再取材的方法,能最大限度保存细胞的微细结构
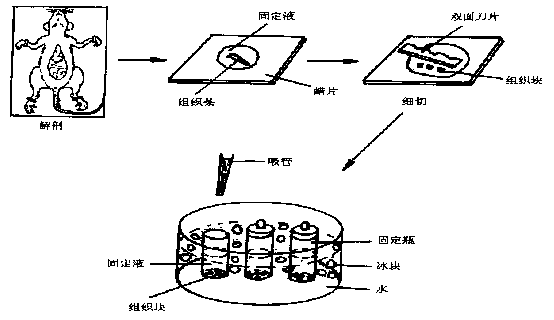
实质性器官:切成正方体小块1mm³
肝脏:切除被膜、切成立方体小块
肾脏:分为皮质与髓质。根据实验要求取相应的部位,切除包膜,切成立方体小块。
肺脏:同肝脏取材,但因肺中含有大量的肺泡及细支气管所以在固定时会漂浮在固定液上,需用针抽真空,使小块完全浸没在固定液中。
有方向性的器官:切成1×1×2 mm³的长方体小块
肠、血管:管腔型组织,在固定时将其剖开,使内膜得以充分的固定。
肌肉、神经:此类组织也存在横切和纵切的差别
心脏:如果可以辨清肌纤维的方向,则按肌肉取材。否则同肝脏取材。
对于脑、肺等对缺血比较敏感的器官及需要同时取多个组织器官尽量采取灌注后取材的方法。
睾丸一类,基膜比较厚,离心脏较远的,或者比较松软的组织,固定难度大,可采用灌注和局部灌注注射固定,用注射针直接插入,从多方向进行固定。
培养细胞的取材方法:
将培养细胞用刮刀刮下,在离心管中低速离心数分钟,弃上清液,缓冲液清洗1-2遍,加入4%多聚甲醛固定数小时,缓冲液冲洗后加入2.5%戊二醛离心后将细胞团块转移到青霉素小瓶中切成1mm3小块继续置于4℃冰箱内固定。(难点:既要减少细胞损伤,又要保证呈致密的团块,在后期处理中不会散开。)
对于不易聚团的细胞,我们可以用琼脂预包埋的方法处理

取材常见问题及注意事项与对策
1、取材组织块过大,固定不好,不能良好保存组织的超微结构,取材一定要小。
2、取材部位不准确,
3、取材方向不明确
4、组织块飘在固定液上
5、贴壁培养细胞主要观察细胞生长状态及细胞间的关系,取材时给刮下来,影响细胞状态观察。对策:细胞应保持在原来支撑物内,原位进行固定、脱水、原位包埋
6、培养细胞不聚团,用琼脂包埋法进行预包埋。
二、 固定
固定的温度一般是在4度或者室温,采用灌注、浸泡或者抽真空浸泡的方式。
试剂:四氧化锇、戊二醛、多聚甲醛
四氧化锇( osmium tetroxide)
固定物质:固定蛋白质、脂肪、脂蛋白、稳定膜结构。不
能固定DNA/RNA及糖原。
特点:渗透力较差、时间不能长、对酶活性破坏性大、价格昂
贵,有剧毒。不适合做电镜细胞化学固定,免疫电镜的
前固定。
浓度、时间:1%~2%,1~2小时
戊二醛( glutaraldehyde)
固定物质:微管、纺锤丝、细胞基质、糖原、核蛋白。不
能保存脂肪。
特点:渗透比较快,可以较长时间固定,不易使酶失活。
浓度、时间:2.5%~4%,时间1小时以上,最长不超过1个月。 多聚甲醛
对致密组织固定作用较好,但是对细胞超微结构保存差, 一般不能单独使用。
脱水剂:乙醇和丙酮
脱水过程:梯度脱水,减少组织因脱水而造成的收缩损伤
50%乙醇→70%乙醇→ 80%乙醇→95%乙醇→100%乙醇→ 100%乙醇→ 100%乙醇→100%丙酮→ 100%丙酮
脱水注意事项:
脱水要彻底;脱水时间不宜太长(10-15min/次);含水多的样品(如海洋生物等)要从更低浓度开始(如30%)
三:浸透与包埋
目的是用包埋剂逐渐取代组织中的脱水剂,使细胞内外所有的空隙都被包埋剂填充。
理想的包埋剂应具备的特点:
1、有良好的硬度和切割性能
2、有足够的低粘度,容易渗入样品
3、能与脱水剂互溶
4、透明度好
5、聚合后体积不变
6、能经受电子束的轰击,高温下不变形
7、本身在电镜高倍放大下不呈现可见结构等
常用的包埋剂:环氧树脂(Epon812、Spurr树脂)
包埋过程:
1份丙酮+1份包埋剂渗透 纯包埋剂渗透 包埋、聚合
渗透与包埋过程中的注意事项:
1、所有器皿都要干净,烘干后自然冷却才可使用
2、包埋剂的配制要充分搅拌
3、包埋过程一定要避免接触水分或者受潮
四、超薄切片
(一)、准备工作:
(1)包埋块的修整(半薄定位)
(2)刀的准备(玻璃刀、钻石刀)
(3)载网、支持膜的准备(铜网)
半薄切片:厚度1um,大小尽量保存整个组织切面。
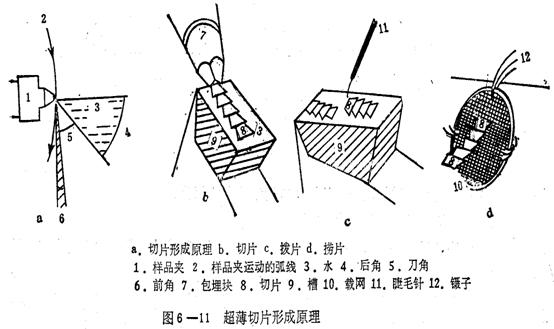
(二)超薄切片的操作步骤:
1、装块2、装刀3、对刀4、加水5、切片和捞片
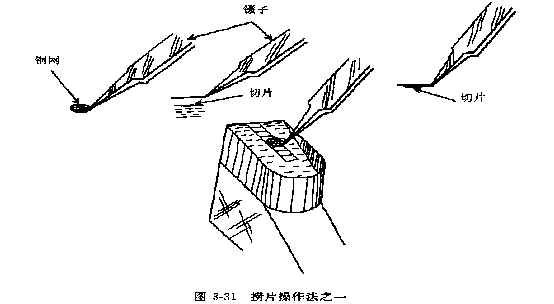
(三)切片的收集(捞片)
切片的厚度可根据干涉色来判断。
– 暗灰色调 40nm
– 灰色 40-50nm,较薄,易被电子束击破
– 银白色 60-70nm,最常用
– 金黄色 70-80nm
– 紫色为 90nm以上,较厚,细节结构不清
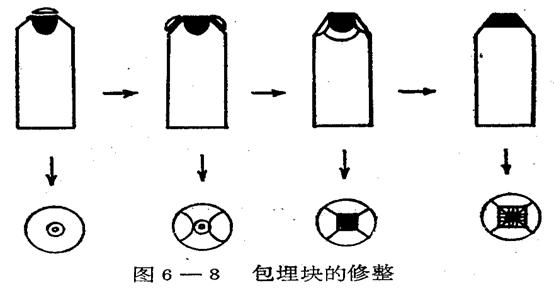
获得良好切片的基本要求:
包埋块软硬度适中、切面面积不宜太大、必须保证有两个边平行、切片机性能稳定、切片刀刀口锋利无损伤、切片速度适中、切片中无振动等等。
理想切片
厚度适中(50-70nm),均匀一致、没有刀痕、颤痕和皱褶。
常见缺陷
刀痕、颤痕、切片重叠、折叠、破碎、污染等。
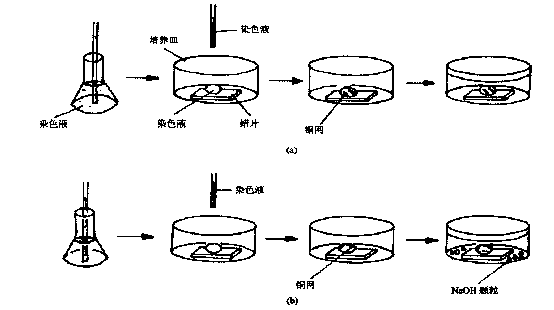
五、染色
染色目的:增强切片上不同成分间的电子反差
常用染色剂:醋酸铀染色液 (染色30min)
柠檬酸铅染色液(染色10min)
染色方式:包埋前染色(块染)
包埋后染色(片染)
染色注意事项:
铀染要避光、铅染要减少接触空气中的CO2
染色常见问题:铀污染、铅污染、混合污染
染色的流程图: